01
CyTOF
单细胞质谱流式
(Mass Cytometry, CyTOF)
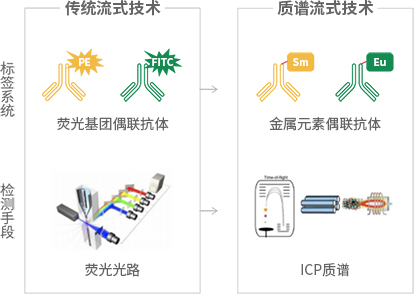
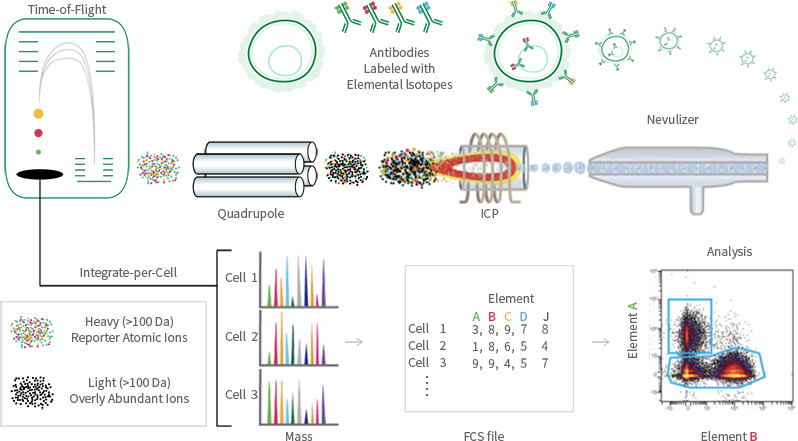
质谱流式细胞技术(Mass Cytometry, CyTOF)结合了飞行时间质谱和流式细胞技术的优势,采 用带有金属同位素标签的抗体对细胞进行标记 (细胞表面和内部的蛋白分子),通过飞行时间质 谱分析各细胞上的标签组成,进行细胞表型和功能精细深入的研究。目前,能够实现单细胞水平 超过40个marker的同步检测,由于CyTOF利用同位素重金属偶联的抗体标记细胞,而不是荧光 染料,因此从本质上突破了传统荧光流式通道数量局限。